¿Qué es un electrón?
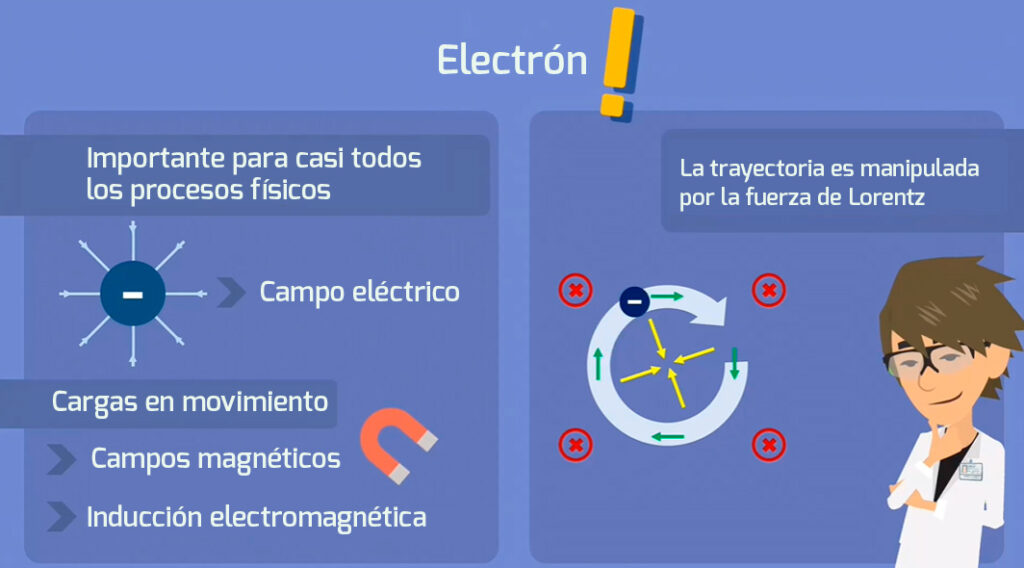
El electrón pertenece a la familia de partículas de los leptones . Hay varias familias diferentes de partículas enumeradas en el Modelo Estándar de física de partículas.
Según los conocimientos actuales, los leptones son partículas elementales . En comparación con otros leptones , el electrón tiene la masa más baja de los leptones portadores de carga. Pertenece a la primera generación de leptones . La segunda y tercera generación forman el muón y el tauón . Estas dos partículas tienen cargas y espín idénticos a los del electrón , pero se diferencian en su masa superior. Los leptones se diferencian de otras partículas fundamentales, como los quarks , por la ausencia de interacción fuerte . Todos los leptones pertenecen a la familia de los fermiones , por eso el electrón tiene un espín de . 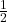
| carga | – 1 y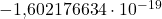 C C |
| masa en reposo | 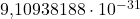 kilos kilos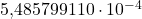 y y |
| Descansa la energía | 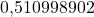 MeVJ MeVJ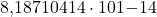 |
| Longitud de onda Compton | 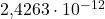 metro metro |
| momento magnético | 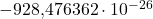 J/T J/T |
| factor g | 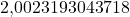 |
| Girar | 1/2 |
| promedio de vida | > 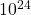 un un |
| interacción | gravedad electromagnética débil |
Tabla de Contenidos
Propiedades del electrón
Además del espín, el electrón se caracteriza por otras propiedades. Su denominada masa invariante es de aproximadamente kilogramos o unidades de masa atómica. Debido a la equivalencia de masa y energía según el principio de la relatividad , esto da como resultado una energía en reposo de 0,511 MeV (megaelectrones voltios). La relación entre la masa de un protón y la de un electrón es 1836. También lleva una carga de Coulomb. El electrón tiene un par intrínseco , o espín , de 1/2. También tiene un momento magnético intrínseco a lo largo del eje de giro. Esto es aproximadamente julios por Tesla.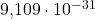
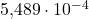
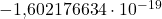
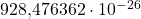
Átomos y moléculas
Los electrones están unidos a los núcleos atómicos mediante la fuerza de atracción de Coulomb . Tal composición de un núcleo atómico y uno o más electrones se llama átomo. Si el número de electrones difiere de la carga nuclear , se trata de un ion . La naturaleza ondulatoria de los electrones unidos se describe mediante los orbitales del átomo . Cada uno de estos orbitales tiene un rango de números cuánticos como energía y par . Además, un átomo sólo puede tener un número discreto de orbitales. Debido al principio de Pauli , en un orbital puede haber un máximo de dos electrones , cuyos espines tienen signos diferentes.
El enlace químico entre átomos se produce mediante interacciones electromagnéticas , que están descritas por la física cuántica . Los enlaces más fuertes se crean al compartir o transferir electrones. Esto permite la formación de moléculas . En las moléculas, los electrones se mueven de manera similar a los átomos y ocupan orbitales moleculares . Sin embargo, una diferencia fundamental es la formación de pares de electrones con espines diferentes. Esto significa que varios electrones ocupan un orbital sin violar el principio de Pauli .
masa de electrones
La masa del electrón se denominó aquí masa invariante . Este término describe la porción de la masa total de un objeto que es independiente del impulso total del sistema circundante. Esto significa que es un valor característico, formado a partir de la energía total y el momento total , que permanece igual en todos los sistemas de referencia. Por tanto, la masa invariante es invariante bajo la transformación de Lorentz .
carga de electrones
El electrón tiene una carga de 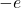 . Esto
. Esto  significa carga elemental . Esta es la cantidad de carga más pequeña que existe libremente. La carga de las partículas libres es cero o un múltiplo entero de
significa carga elemental . Esta es la cantidad de carga más pequeña que existe libremente. La carga de las partículas libres es cero o un múltiplo entero de  . Por tanto, los electrones y muones tienen cargas de
. Por tanto, los electrones y muones tienen cargas de 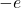 partículas como los protones
partículas como los protones 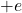 .
.
Energía electrónica
La energía del electrón se calcula a partir de la equivalencia de masa y energía. Esto lo conoces como la fórmula de la teoría de la relatividad 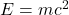 .
. 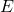 Representa la energía,
Representa la energía, 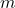 la masa y
la masa y  la velocidad de la luz.
la velocidad de la luz.
Conductividad electrónica
La conductividad de un medio depende de la libertad con la que los electrones pueden moverse en ese medio. En un conductor , los electrones externos de los átomos están en gran medida libres y pueden moverse entre los átomos de manera similar a un líquido . En un aislante, los electrones están unidos a sus átomos de forma estacionaria, lo que limita gravemente su libertad de movimiento. Estos electrones sólo pueden liberarse mediante el suministro de energía (por ejemplo, aumentando la temperatura). Los semiconductores son una forma especial : tienen dos bandas de energía , la banda de valencia y la banda de conducción . Dependiendo del dopaje y de la temperatura del semiconductor, estos pueden utilizarse como conductores o aislantes.
Electrones, protones, neutrones.
Es importante que conozcas la diferencia entre los tres nucleones más importantes.
Primero el electrón . Se trata de una partícula elemental cargada negativamente con espín 1/2 y masa muy baja. Los electrones forman la capa atómica alrededor de un núcleo atómico. En los átomos neutros, el número de electrones que contienen es igual al número de protones en el núcleo.
El protón no es una partícula elemental. Está compuesto por tres quarks y tiene carga positiva . Junto con los neutrones, los protones forman el núcleo de un átomo. En conjunto, estos se denominan nucleidos .
El neutrón también está formado por tres quarks . Sin embargo, su composición hace que el neutrón esté descargado, es decir, neutro. Los neutrones son importantes para la estabilidad de un núcleo atómico.
Al igual que el electrón, los protones y neutrones también tienen un espín de 1/2. Por tanto, también pertenecen a la familia de los fermiones.






